高中有机化学重要规律及应用总结!
发布于 2021-04-12 15:56 ,所属分类:知识学习综合资讯

一、有机物的通式规律
随C原子个数的递增,找出其中的“重复单元”从而得出通式。
烷烃:重复单元为“CH2”,n个CH2,再加2个H,即CnH2n+2
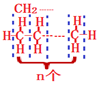
烯烃:在烷烃的基础出少2个H,即CnH2n
环烷:去掉烷两端的H,形成一个环,即CnH2n
炔烃:在烷烃的基础出少4个H,相当于形成2个双键,即CnH2n-2
苯环:相当于已烷去掉6个H,形成三个C=C双键,再去掉2H形成个环,因此苯的同系物为CnH2n-6,苯的同系数物也为CnH2n-6
如下各种烃的通式找法:
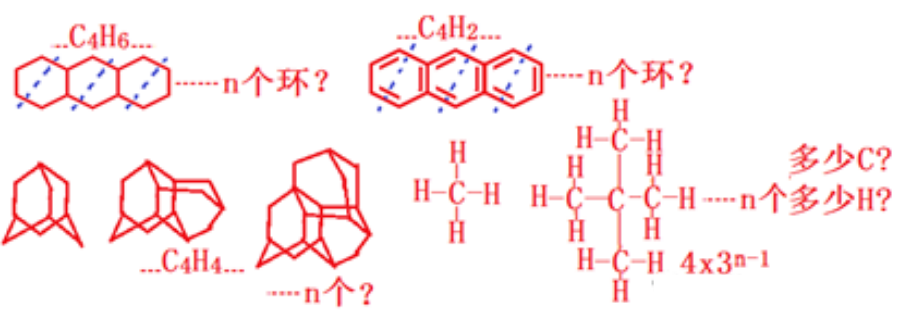
二、烃中C、H的百分含量
烃的通式为CnH2n±X,因此,n趋近于无穷大量,极值均为CnH2n.即:
烷烃越大,含C数越高,含氢量越低;烯烃不变;
炔烃或芳烃,含C数越多,含C量越少,含H越高,极值均为烯。即:
含碳规律:小烷<大烷<烯<大炔<小炔;含H反之同理。
CH4:C%=75% H%=25
C2H4: C%=85.7H%=14.3%
C2H2: C%=92.3H%=7.7% 各种烃的n增大的C%趋近于烯CH2
三、不饱和度计算及应用
不饱和度:即与烷烃(饱和烃)相比的缺H对数。
由于O是2价元素,形成两个键,-O-可插入链中,不影响不饱和度;
卤素形成一个键,-X认为是代替的一个H,因此有卤素原子按H计算;
由于N原子形成三键-N=,因此有N原子时,相当于插入时代入一个H,因此有N时应加一个H,同时注意-NO2有一双键。
不饱和度的分子式计算如下:
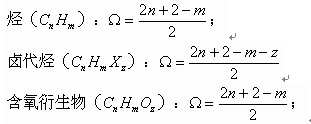
有机物结构与不饱和度关系:
Ω=0,烷烃;
Ω=1,双键(包括C=C、C=0、C=N-)或单环
Ω=2,说明分子中有两个双键或一个三键;
或一个双键和一个环;或两个环;其余类推
Ω≥4,一般认为是苯环。当然也可是双键、环、三键等组合。
说明:立体环状烷不饱和度Ω=所有立体环数-1.
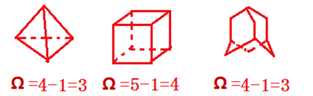
四、 有机物燃烧耗氧通式为
1、摩耗氧量:
CxHy



![高中化学常考100个重要知识点总结![百度网盘分享]](https://static.kouhao8.com/cunchu/cunchu7/2023-05-18/UpFile/defaultuploadfile/230430ml/138-1.jpg?x-oss-process=image/format,webp/resize,w_88/crop,w_88,h_88,g_nw)



![高中重要知识点汇集,全面梳理备考![百度网盘分享]](https://static.kouhao8.com/cunchu/cunchu7/2023-05-18/UpFile/defaultuploadfile/230430ml/208-1.jpg?x-oss-process=image/format,webp/resize,w_88/crop,w_88,h_88,g_nw)

![高中地理16种地貌知识点总结![百度云资源]](https://static.kouhao8.com/cunchu/cunchu7/2023-05-18/UpFile/defaultuploadfile/230505ml3/7-1.jpg?x-oss-process=image/format,webp/resize,w_88/crop,w_88,h_88,g_nw)
相关资源